Znanost je stopila na novo, vznemirljivo in hkrati skrb vzbujajočo pot. Z napredkom tehnologije, kot je CRISPR, ki omogoča izjemno natančne posege v DNK, se odpirajo vrata v svet, kjer bi lahko preprečili marsikatero dedno bolezen. Vendar pa ta tehnološki preboj prinaša s seboj tudi globoke etične dileme in neznana tveganja za prihodnje generacije. Milijarderji iz Silicijeve doline vse bolj vlagajo v zagonska podjetja, ki si prizadevajo za gensko spreminjanje človeških zarodkov, kar nakazuje smer prihodnjih raziskav, kljub temu da so posledice še vedno zelo nejasne.
Korenine Revolucije: Primer He Jiankuija
Zgodba o genskem spreminjanju človeških zarodkov je močno zaznamovana s primerom kitajskega znanstvenika He Jiankuija. Leta 2018 je šokiral svet z razkritjem, da je skrivaj ustvaril prve gensko spremenjene dojenčke. Njegov cilj je bil z uporabo metode CRISPR onesposobiti gen, ki omogoča vstop virusa HIV v celico, s čimer naj bi deklici postali odporni proti okužbi. V ta namen je spremenil DNK zarodkov osmih parov, pri čemer so očetje imeli HIV, matere pa ne. Umetna oploditev je bila uspešna le pri dvojčicah.
Ta eksperiment je sprožil plaz neodobravanja po vsem svetu. Njegova univerza je javno zanikala poznavanje njegovih dejavnosti, ga obsodila kot "resno kršitev akademske etike in standardov" in ga suspendirala. Michael Deem, profesor bioinženiringa na univerzi Rice, ki je sodeloval pri projektu, se je znašel pod preiskavo. Tudi tisti, ki so sicer naklonjeni genskemu spreminjanju človeka, kot je profesor Julian Savulescu z Oxfordske univerze, so Hejev poskus označili kot "nezaslišan", saj je zdrave otroke izpostavil tveganjem brez realne potrebe, s čimer je kršil desetletja etičnih soglasij in smernic za zaščito udeležencev pri raziskavah. V mnogih državah bi bili takšni posegi nezakoniti in bi vodili v zaporno kazen. He Jiankuija so zaradi njegovega dejanja kasneje doleteli tudi sodni postopki in zaporna kazen, ki je temeljila na "nelegalnih medicinskih praksah".
Pomembno je poudariti, da je bil Hejev poskus izveden proti etičnim standardom in je bil marsikje nezakonit. Znanstvenik je deloval v nasprotju z veljavnimi predpisi, zbral finančna sredstva zasebno in se izognil nadzoru svoje univerze. Preiskava v provinci Guangdong je pokazala, da je He ponaredil dokumente in se namerno izognil nadzoru, pri čemer je organiziral zasebno ekipo za izvedbo projekta. Njegovi motivaciji naj bi bila predvsem slava in osebna korist, čeprav so nekateri namigovali, da naj bi bil projekt odobren s strani "back-enda" komunistične partije, zlasti glede na razširjenost virusa HIV na Kitajskem.
Dodatno zapletenost primeru dodaja dejstvo, da je He Jiankui kasneje namignil na še eno nosečnost z gensko spremenjenim zarodkom. Ameriški zdravnik William Hurlbut, ki se ukvarja z bioetiko na Univerzi Stanford in je bil v stiku s Hejem, je potrdil, da je bila ena od udeleženk v njegovem poizkusu noseča med 12. in 14. tednom. Kljub temu, da je bilo v času Hejeve objave konec novembra še prezgodaj za ultrazvočno zaznavo zarodka, je bilo mogoče njegovo prisotnost zaznati kemično. Hurlbut je poudaril, da je bil He po objavi novice o dvojčicah "pod nadzorom varnostnikov", kar je omejilo njuno neposredno srečevanje, a sta ostala v stiku preko elektronske pošte in telefona.
He Jiankuijev primer, čeprav izveden na sporen in nezakonit način, je odprl vrata razpravam o potencialu in tveganjih genskega spreminjanja zarodkov.
Nova Era: Vstop Kapitala in Tehnološki Napredek
Konec oktobra je ameriški startup Preventive objavil, da razvija tehnologijo za gensko spreminjanje človeških zarodkov s pomočjo tehnike CRISPR. Njihov ustanovitelj Lucas Harrington je na platformi X sporočil, da so zbrali 30 milijonov dolarjev, med vlagatelji pa sta direktor Coinbasea Brian Armstrong in Oliver Mulherin, mož Sama Altmana, vodje OpenAI. Harrington sicer trdi, da se bo podjetje sprva osredotočilo na raziskave varnosti z namenom preprečevanja hudih dednih bolezni.
Preventive ni edini z ambicioznimi načrti. Podobne cilje imajo tudi druga podjetja, kot sta Manhattan Genomics in Bootstrap Bio. Vstop kapitala vlagateljev, kot so milijarderji iz Silicijeve doline, močno nakazuje, kam se usmerjajo prihodnje raziskave, kljub temu da gre za eno najspornejših tem v sodobni medicini.
Tehnologija CRISPR, ki sta jo leta 2012 zasnovali Jennifer Doudna in Emmanuelle Charpentier (za kar sta prejeli Nobelovo nagrado), omogoča izjemno natančne posege v DNK. Vendar pa uporaba te tehnologije še vedno prinaša znatna tveganja. CRISPR ustvarja prelom v DNK, celica pa ta poškodovanja poskuša popraviti, pogosto nepopolno. Posledična popravila lahko ustvarijo nove mutacije ali nepričakovane spremembe, katerih učinki so težko predvidljivi.
Kljub temu zagovorniki raziskav na tem področju poudarjajo potencialne prednosti. Spreminjanje zarodkov bi bilo teoretično cenejše in učinkovitejše kot obstoječe genske terapije, saj bi se popravljene spremembe razširile v vsa tkiva razvijajočega se organizma. Trenutno prvo odobreno zdravljenje, Casgevy, za srpastocelično anemijo, je na primer izredno drago, s ceno okoli dva milijona dolarjev, in ima znatne pomanjkljivosti pri dostavi urejenega genskega materiala v telo ter je dolgotrajno.
Harrington sicer zatrjuje, da se Preventive ukvarja le z boleznimi. Vendar pa pot naprej lahko hitro vodi od popravljanja mutacij do ustvarjanja "zaščitnih" genov proti boleznim, kot sta rak ali demenca, ter nato do ponudb za izboljšave videza, inteligence ali drugih značilnosti otrok. Ta premik od zdravljenja k izboljšavam je tista meja, ki skrbi regulatorje in znanstveno skupnost.
Navigacija po Etiki in Regulaciji
Znanstvena skupnost večinoma še vedno nasprotuje genskemu spreminjanju zarodkov, čeprav se, kot pravi razvojni biolog Robin Lovell-Badge, soglasje lahko spremeni. Napredek v različicah CRISPR, zlasti tako imenovano urejanje baze (angl. base editing), ki DNK ne prereže v celoti, daje obetavne rezultate. Ta tehnika bi lahko omogočila bolj ciljane in varnejše popravke genetskih napak.
Vendar pa se kljub napredku pojavljajo pomisleki. Britanska pristojna agencija je že posvarila, da bi lahko takšni poskusi obudili številne etične razprave. V Veliki Britaniji je sicer gensko spreminjanje človeškega genoma v nekaterih primerih zakonito, kar je potrdil tudi nedavni zakon, ki omogoča, da imajo otroci lahko tri biološke starše. Pred letom dni smo dobili prve hibride med ljudmi in živalmi, katerih obstoj znanstveniki upravičujejo s potrebo po človeških organih, ki jih s pomočjo živali in mešanjem genskega zapisa že gojijo v laboratorijih.
Čeprav je gensko spreminjanje zarodkov pogosta praksa v znanstvenih laboratorijih za raziskovalne namene, je rojstvo otrok s spremenjenim genom pri večini držav prepovedano. Vendar pa se pojavljajo ideje o možnostih v državah, ki morda nimajo tako strogih regulacij. Ameriška agencija za hrano in zdravila (FDA) na primer takšnih poskusov ne sme niti vzeti v obzir. Kljub temu Harrington trdi, da je "prehitro razmišljati o kateri koli jurisdikciji", kar nakazuje na potencialno globalno širitev teh raziskav.
V Združenem kraljestvu se bo v britanskem parlamentu čez nekaj dni odvijala razprava o etičnosti takšnih raziskav. Obstaja velika verjetnost, da bodo poslanci dovolili ustvarjanje gensko spremenjenih zarodkov, kar bi lahko pomenilo nov mejnik v tej občutljivi debati.
Znanstvene Podlage in Izzivi
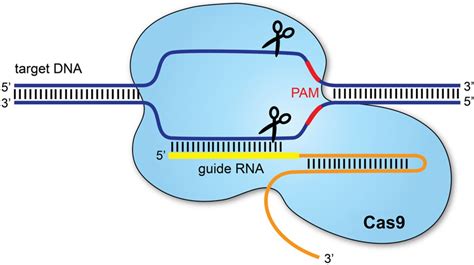
Tehnologija CRISPR-Cas9 deluje kot molekularne škarje, ki lahko na natančno določenem mestu prerežejo verigo DNK. To omogoča izločanje neželenih genov ali njihovo zamenjavo z želenimi. Znanstveniki uporabljajo različne pristope, vključno z vnosom gena v zarodek preko virusa, kot je to storila ekipa, ki jo vodi Nikica Zaninovic. Vendar pa ta ekipa ni imela dovoljenja za spremljanje nadaljnjega razvoja zarodka, kar poudarja težave z regulacijo in nadzorom.
Eden od ključnih izzivov ostaja zanesljivost metode. Poleg ciljne spremembe lahko CRISPR uvede tudi neželene mutacije na drugih lokacijah v genomu, kar lahko vodi do nepričakovanih posledic. Urejanje baze (base editing) je naprednejša oblika CRISPR, ki ne prereže celotne DNK, temveč neposredno spremeni posamezne baze, kar naj bi bilo varnejše. Vendar pa so tudi te tehnike še v zgodnji fazi razvoja.
Primer rusko govorečega znanstvenika Denisa Reberikova, ki javno izraža namen uporabe CRISPR za odpravo dedne gluhosti pri petih gluhotrpnih parov, ponuja drugačen pogled. Medtem ko so tveganja podobna kot pri kitajskem primeru, je prednost pri ruskih poskusih bolj jasna - odprava gotovega stanja, ki bistveno vpliva na kakovost življenja, v primerjavi s preprečevanjem potencialne okužbe s HIV kot pri He Jiankuiju. Reberikov namerava zaprositi za dovoljenja, kar predstavlja bolj transparenten pristop.
Vendar pa tudi v primeru Reberikova obstajajo etični pomisleki. Nekateri predstavniki gluhotrpne skupnosti gluhote ne dojemajo kot invalidnosti, temveč kot del svoje kulture in identitete. Zato se poraja vprašanje, ali je spreminjanje genov, ki bi povzročili ali odpravili gluhoto, sploh etično sprejemljivo, če obstaja skupnost, ki to sprejema kot del svoje identitete.
Dolgoročne Posledice in Prihodnost
Spreminjanje človeške DNK, zlasti na zarodni stopnji, ima potencialne dolgoročne posledice, ki segajo daleč preko posameznika. Te spremembe so dedne in se bodo prenašale na prihodnje generacije. To postavlja vprašanje, ali si kot družba lahko privoščimo sprejemati odločitve, ki bodo vplivale na genetsko dediščino človeštva za nedoločen čas.
Obstaja skrb, da bi lahko gensko spreminjanje vodilo v ustvarjanje "oblikovanih otrok" (designer babies), kjer bi se starši odločali za genetske izboljšave, kot so višja inteligenca, boljši fizični videz ali odpornost proti boleznim. To bi lahko vodilo do novih oblik neenakosti in diskriminacije, kjer bi tisti, ki si lahko privoščijo takšne posege, postali genetsko "boljši" od tistih, ki si jih ne morejo.
Robert Edwards, pionir umetne oploditve, je nekoč dejal: "Kmalu bo greh za starše, da imajo otroka, ki nosi težko breme genetske bolezni. Vstopamo v svet, kjer moramo upoštevati kakovost naših otrok." Njegove besede odsevajo premik v razmišljanju, vendar pa istočasno odpirajo vrata vprašanjem o tem, kdo določa "kakovost" in kakšne so posledice takšnega razmišljanja.
Čeprav je tehnologija CRISPR in sorodne metode izjemno obetavna za zdravljenje dednih bolezni, je ključno, da se raziskave izvajajo varno, etično in pod skrbnim nadzorom. Vstop kapitala v to področje zahteva še večjo previdnost, da se prepreči nepremišljeno ali neetično izkoriščanje te močne tehnologije. Svet se premika proti nečemu, kar se je še pred nekaj leti zdelo nedotakljivo, a vprašanja o varnosti, etiki in dolgoročnih posledicah ostajajo osrednja. Ali lahko varno spreminjamo človeško DNK in kakšna bo prihodnost človeške evolucije, ostaja odprto vprašanje.
tags: #gensko #spremenjen #zarodek
